Mga kategorya: Itinatampok na Mga Artikulo » Mga bagyong elektrisista
Bilang ng mga tanawin: 52646
Mga puna sa artikulo: 4
Mga Transistor Bahagi 2. Mga conductor, insulators at semiconductors
Simula ng artikulo: Kasaysayan ng transistor, Transistor: layunin, aparato at mga prinsipyo ng pagpapatakbo
 Sa electrical engineering, ginagamit ang iba't ibang mga materyales. Ang mga de-koryenteng katangian ng mga sangkap ay natutukoy ng bilang ng mga elektron sa panlabas na orbit ng valence. Ang mas kaunting mga electron ay nasa orbit na ito, ang mas mahina sila ay nauugnay sa nucleus, mas madali silang makapunta sa paglalakbay.
Sa electrical engineering, ginagamit ang iba't ibang mga materyales. Ang mga de-koryenteng katangian ng mga sangkap ay natutukoy ng bilang ng mga elektron sa panlabas na orbit ng valence. Ang mas kaunting mga electron ay nasa orbit na ito, ang mas mahina sila ay nauugnay sa nucleus, mas madali silang makapunta sa paglalakbay.
Sa ilalim ng impluwensya ng pagbabagu-bago ng temperatura, ang mga elektron ay lumayo mula sa atom at lumipat sa interatomic space. Ang ganitong mga elektron ay tinatawag na libre, at lumikha sila ng isang electric current sa mga conductor. Mayroon bang isang malaking interatomic space, mayroon bang silid para sa mga libreng elektron na maglakbay sa loob ng bagay?
Ang istraktura ng mga solido at likido ay tila tuluy-tuloy at siksik, na nakapagpapaalala sa istruktura ng isang bola ng thread. Ngunit sa katunayan, kahit na ang solido ay katulad ng pangingisda o volleyball net. Siyempre, hindi ito makikilala sa antas ng sambahayan, ngunit naitatag ito ng tumpak na pag-aaral sa siyensiya na ang mga distansya sa pagitan ng mga electron at ang nucleus ng mga atom ay mas malaki kaysa sa kanilang sariling mga sukat.
Kung ang laki ng atomic nucleus ay kinakatawan sa anyo ng isang bola ang laki ng isang soccer ball, kung gayon ang mga electron sa modelong ito ay ang laki ng isang gisantes, at ang bawat naturang gisantes ay matatagpuan mula sa "core" sa layo na ilang daan at kahit libu-libong metro. At sa pagitan ng nucleus at electron ay kawalan ng laman - walang simpleng bagay! Kung naiisip natin ang mga distansya sa pagitan ng mga bagay na mahalaga sa parehong sukat, ang mga sukat ay magiging pangkalahatang kamangha-manghang - sampu-sampung daan-daang kilometro!
Magandang conductors ng koryente ay metal. Halimbawa, ang mga atom ng ginto at pilak ay may isang elektron lamang sa panlabas na orbit, samakatuwid sila ang pinakamahusay na conductor. Ang bakal ay nagsasagawa rin ng koryente, ngunit bahagyang mas masahol.
Magsagawa ng kuryente kahit na mas masahol pa mataas na pagtutol na haluang metal. Ang mga ito ay nichrome, manganin, constantan, fechral at iba pa. Ang nasabing iba't ibang mga haluang metal na resistensya ay dahil sa ang katunayan na sila ay dinisenyo upang malutas ang iba't ibang mga problema: mga elemento ng pag-init, mga sukat ng pilay, mga risistor ng sanggunian para sa pagsukat ng mga instrumento, at marami pa.
Upang masuri ang kakayahan ng isang materyal na magsagawa ng koryente, ang konsepto ng "Electrical conductivity". Ang halaga ng pagbabalik ay resistivity. Sa mga mekanika, ang mga konsepto na ito ay tumutugma sa tiyak na gravity.
Mga insulator, hindi katulad ng mga conductor, ay hindi gaanong mawalan ng mga electron. Sa kanila, ang bono ng elektron na may nucleus ay napakalakas, at halos walang libreng mga electron. Mas tiyak, ngunit kakaunti. Kasabay nito, sa ilang mga insulators mayroong higit pa sa kanila, at ang kanilang kalidad ng pagkakabukod ay, nang naaayon, mas masahol pa. Ito ay sapat na upang ihambing, halimbawa, keramika at papel. Samakatuwid, ang mga insulator ay maaaring kondisyon na nahahati sa mabuti at masama.
Ang hitsura ng mga walang bayad na singil kahit sa mga insulator ay dahil sa mga thermal vibrations ng mga electron: sa ilalim ng impluwensya ng mataas na temperatura, ang mga katangian ng insulating ay lumala, ang ilang mga electron ay pinamamahalaan pa ring lumayo mula sa nucleus.
Katulad nito, ang resistivity ng isang mainam na conductor ay magiging zero. Ngunit sa kabutihang palad ay walang ganoong conductor: isipin kung ano ang batas ng Ohm ((I = U / R) na magmumukha ng zero sa denominador !!! Paalam sa matematika at elektrikal na inhinyero.
At lamang sa isang ganap na temperatura ng zero (-273.2 ° C) ang thermal fluctuations ay ganap na huminto, at ang pinakamasama insulator ay nagiging sapat na mabuti. Upang matukoy ang bilang na "ito" ay masama - mahusay na gamitin ang konsepto ng resistivity. Ito ang paglaban sa Ohms ng isang kubo na may haba na gilid ng 1 cm, ang sukat ng resistivity ay nakuha sa ohms / cm. Ang tiyak na paglaban ng ilang mga sangkap ay ipinapakita sa ibaba.Ang konduktibo ay ang timpla ng resistivity, ay ang yunit ng pagsukat ng Siemens, - 1Sm = 1 / Ohm.
Mayroon silang mahusay na kondaktibiti o mababang resistivity: pilak 1.5 * 10 ^ (- 6), basahin kung paano (isa at kalahati hanggang sampu hanggang sa kapangyarihan minus anim), tanso 1.78 * 10 ^ (- 6), aluminyo 2.8 * 10 ^ (- 6). Ang kondaktibo ng mga haluang metal na may mataas na pagtutol ay mas masahol pa: constantan 0.5 * 10 ^ (- 4), nichrome 1.1 * 10 ^ (- 4). Ang mga haluang metal na ito ay maaaring tawaging masamang conductor. Matapos ang lahat ng mga kumplikadong numero, palitan ang Ohm / cm.
Dagdag dito, sa isang hiwalay na grupo, ang mga semiconductor ay maaaring makilala: germanium 60 Ohm / cm, silikon 5000 Ohm / cm, seleniyum 100 000 Ohm / cm. Ang resistivity ng pangkat na ito ay mas malaki kaysa sa mga masasamang conductor, ngunit mas mababa kaysa sa mga masamang insulator, hindi masabi ang mabubuti. Marahil, sa parehong tagumpay, ang mga semiconductor ay maaaring tawaging semi-insulators.
Matapos ang tulad ng isang maikling kakilala sa istraktura at mga katangian ng isang atom, dapat isaalang-alang ng isa kung paano nakikipag-ugnay ang mga atomo sa bawat isa, kung paano nakikipag-ugnay ang mga atomo sa bawat isa, kung paano ang mga molekula ay gawa sa kanila, kung saan binubuo ang iba't ibang mga sangkap. Upang gawin ito, kakailanganin mong alalahanin ang mga electron sa panlabas na orbit ng atom. Pagkatapos ng lahat, ito ang mga nakikilahok sa pagbubuklod ng mga atomo sa mga molekula at matukoy ang mga pisikal at kemikal na katangian ng bagay.
Paano ang mga atomo ay ginawa mula sa mga atomo
Ang anumang atom ay nasa isang matatag na estado kung mayroong 8 elektron sa panlabas na orbit nito. Hindi niya hinahangad na kumuha ng mga elektron mula sa mga kalapit na atomo, ngunit hindi niya isusuko ang kanyang sarili. Upang mapatunayan ito, sapat na sa pana-panahong talahanayan upang tumingin sa mga gas na hindi gumagalaw: neon, argon, krypton, xenon. Ang bawat isa sa kanila ay may 8 elektron sa panlabas na orbit, na nagpapaliwanag ng pag-aatubili ng mga gas na ito upang makapasok sa anumang relasyon (mga reaksyon ng kemikal) kasama ang iba pang mga atom, upang makabuo ng mga molekula ng mga kemikal.
Ang sitwasyon ay ganap na naiiba para sa mga atoms na walang 8 itinatangi na mga electron sa kanilang panlabas na orbit. Ang ganitong mga atomo ay ginusto na magkaisa sa iba upang madagdagan ang kanilang panlabas na orbit na may hanggang 8 na mga electron at makahanap ng isang mahinahon na matatag na estado.
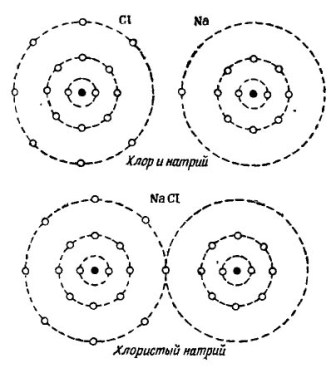
Halimbawa, ang kilalang molekula ng tubig na H2O. Binubuo ito ng dalawang atom ng hydrogen at isang atom na oxygen, tulad ng ipinapakita sa figure. 1.
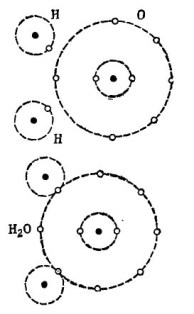
Pagguhit 1. Paano nilikha ang isang molekula ng tubig.
Sa itaas na bahagi ng figure, dalawang hydrogen atoms ang isang oxygen na atom ay ipinapakita nang hiwalay. Mayroong 6 na mga electron sa panlabas na orbit ng oxygen at dalawang elektron sa dalawang mga hydrogen atoms ay malapit. Ang oksiheno hanggang sa itinatangi na numero 8 ay nawawala lamang ng dalawang elektron sa panlabas na orbit, na tatanggapin niya sa pamamagitan ng pagdaragdag ng dalawang atom ng hydrogen sa kanyang sarili.
Ang bawat hydrogen atom ay walang 7 electron sa panlabas na orbit nito para sa kumpletong kaligayahan. Ang unang hydrogen atom na natatanggap sa panlabas na orbit na 6 na mga electron mula sa oxygen at isa pang elektron mula sa kambal nito - ang pangalawang hydrogen atom. Mayroon na ngayong 8 elektron sa panlabas na orbit nito kasama ang elektron nito. Ang ikalawang hydrogen atom ay nakumpleto rin ang panlabas na orbit nito sa coveted number 8. Ang prosesong ito ay ipinapakita sa mas mababang bahagi ng figure. 1.
Sa larawan 2 Ang proseso ng pagsasama-sama ng mga atomo ng sodium at chlorine ay ipinakita. Ang resulta ay sodium chloride, na ibinebenta sa mga tindahan na tinatawag na asin.
Pagguhit 2. Ang proseso ng pagsasama ng mga atomo ng sodium at klorin
Dito rin, ang bawat isa sa mga kalahok ay natatanggap ang nawawalang bilang ng mga electron mula sa iba: ang klorin ay nakakabit ng isang solong sodium elektron sa sarili nitong pitong elektron, habang binibigyan nito ang mga atomo nito sa sodium atom. Ang parehong mga atomo sa panlabas na orbit ay may 8 elektron, kung saan nakamit ang buong kasunduan at kaunlaran.
Katatagan ng mga atomo
Ang mga atom na may 6 o 7 na mga electron sa kanilang panlabas na orbit ay may posibilidad na maglakip ng 1 o 2 elektron sa kanilang sarili. Sinasabi nila ang tungkol sa gayong mga atomo na sila ay isa o divalent. Ngunit kung sa panlabas na orbit ng isang atom 1, 2 o 3 na mga electron, kung gayon ang tulad ng isang atom ay may kaugaliang ibigay sa kanila. Sa kasong ito, ang atom ay itinuturing na isa, dalawa o trivalent.
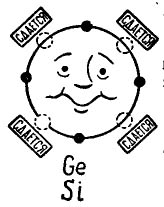
Kung mayroong 4 na mga electron sa panlabas na orbit ng isang atom, kung gayon ang tulad ng isang atom ay mas gusto na pagsamahin sa parehong isa, na mayroon ding 4 na mga electron. Ito ay kung paano pinagsama ang mga atom ng germanium at silikon sa paggawa ng mga transistor. Sa kasong ito, ang mga atomo ay tinatawag na tetravalent. (Ang mga atom ng germanium o silikon ay maaaring pagsamahin sa iba pang mga elemento, halimbawa, oxygen o hydrogen, ngunit ang mga compound na ito ay hindi kawili-wili sa plano ng aming kuwento.)
Sa larawan 3 ang isang germanium o silikon na atom ay ipinapakita na nais na pagsamahin sa parehong atom. Ang mga maliliit na itim na bilog ay ang sariling mga elektron ng atom, at ang mga ilaw na bilog ay nagpapahiwatig ng mga lugar kung saan ang mga elektron ng apat na mga atom - mga kapitbahay - nahuhulog.
Pagguhit 3. Atom ng germanium (silikon).
Ang istraktura ng kristal ng semiconductors
Ang mga atomo ng germanium at silikon sa pana-panahong talahanayan ay nasa parehong pangkat na may carbon (ang kemikal na pormula ng diamante C ay simpleng malalaking kristal na kristal na nakuha sa ilalim ng ilang mga kundisyon), at samakatuwid, kapag pinagsama, bumubuo ng isang istraktura na tulad ng kristal na tulad ng diyamante. Ang pagbuo ng tulad ng isang istraktura ay ipinapakita, sa isang pinasimple, siyempre, form sa figure 4.
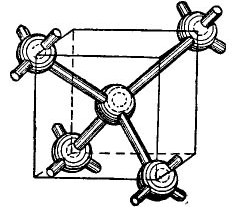
Pagguhit 4.
Sa gitna ng kubo ay isang atom na germanium, at 4 pang mga atoms ang matatagpuan sa mga sulok. Ang atom na inilalarawan sa gitna ng kubo ay nakatali sa pamamagitan ng mga valon ng mga elektron sa pinakamalapit nitong kapitbahay. Kaugnay nito, ang mga anggulo ng anggulo ay nagbibigay sa kanilang mga elektron ng valence sa atom na matatagpuan sa gitna ng kubo at mga kapitbahay nito - mga atomo na hindi ipinapakita sa figure. Kaya, ang mga panlabas na orbit ay pupunan ng hanggang sa walong elektron. Siyempre, walang kubo sa lattice ng kristal, ipinapakita lamang ito sa figure upang ang mutual, volumetric na pag-aayos ng mga atoms ay malinaw.
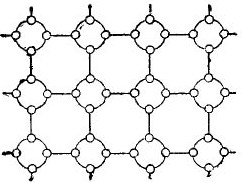
Ngunit upang gawing simple ang kuwento tungkol sa mga semiconductors hangga't maaari, ang kristal na sala-sala ay maaaring kinakatawan sa anyo ng isang patag na pagguhit ng eskematiko, sa kabila ng katotohanan na ang mga interatomic bond ay gayunpaman ay matatagpuan sa espasyo. Ang nasabing circuit ay ipinapakita sa figure. 5.
Pagguhit 5. Ang germanium crystal na sala-sala sa isang flat form.
Sa tulad ng isang kristal, ang lahat ng mga electron ay mahigpit na nakakabit sa mga atoms sa pamamagitan ng kanilang mga bono ng valence, samakatuwid, tila, walang mga libreng elektron dito. Ito ay lumiliko na sa harap natin ay isang insulator sa pigura, dahil walang mga libreng elektron sa loob nito. Ngunit, sa katunayan, hindi ganito.
Intrinsic conductivity
Ang katotohanan ay sa ilalim ng impluwensya ng temperatura, ang ilang mga electron ay pinamamahalaan pa ring lumayo sa kanilang mga atomo, at sa ilang oras ay palayain ang kanilang sarili mula sa bono na may nucleus. Samakatuwid, ang isang maliit na halaga ng mga libreng elektron sa isang kristal na germanium ay umiiral, dahil sa kung saan posible na magsagawa ng isang electric current. Gaano karaming mga libreng elektron ang umiiral sa isang kristal ng germanium sa ilalim ng normal na mga kondisyon?
Hindi hihigit sa dalawang tulad ng mga libreng elektron bawat 10 ^ 10 (sampung bilyong) mga atom, kaya ang germanium ay isang mahinang conductor, o tulad ng kaugalian na sabihin ng isang semiconductor. Dapat pansinin na ang isang gramo lamang ng germanium ay naglalaman ng 10 ^ 22 (sampung libong bilyon) na mga atom, na nagpapahintulot sa iyo na "makakuha" ng halos dalawang libong bilyon na libreng elektron. Tila sapat na upang makapasa ng isang malaking electric current. Upang harapin ang isyung ito, sapat na upang maalala kung ano ang isang kasalukuyang ng 1 A.
Isang kasalukuyang ng 1 Ang isang katumbas sa pagpasa sa isang conductor sa isang segundo isang singil ng kuryente ng 1 Coulomb, o 6 * 10 ^ 18 (anim na bilyong bilyon) na mga electron bawat segundo. Laban sa background na ito, ang dalawang libong bilyong libreng elektron, at kahit na nakakalat sa isang malaking kristal, ay hindi malamang na matiyak na ang pagpasa ng mga mataas na alon. Bagaman, dahil sa thermal motion, umiiral ang maliit na kondaktibiti sa Alemanya. Ito ang tinatawag na intrinsic conductivity.
Ang conductivity ng electronic at hole
Habang tumataas ang temperatura, ang karagdagang enerhiya ay inilipat sa mga elektron, ang kanilang mga panginginig ng boses ay nagiging mas masigla, bilang isang resulta kung saan pinamamahalaan ng ilang mga elektron na lumayo sa kanilang mga atomo.Ang mga electron na ito ay nagiging libre at, kung wala ang isang panlabas na electric field, gumawa ng magulong galaw at lumipat sa libreng espasyo.
Ang mga atom na nawalan ng mga electron ay hindi maaaring gumawa ng mga random na paggalaw, ngunit bahagyang mag-oscillate na kamag-anak lamang sa kanilang normal na posisyon sa kristal na lattice. Ang ganitong mga atomo, na nawalan ng mga electron, ay tinatawag na mga positibong ion. Maaari nating ipalagay na sa lugar ng mga electron na napunit mula sa kanilang mga atomo, ang mga libreng puwang ay nakuha, na karaniwang tinatawag na mga butas.
Sa pangkalahatan, ang bilang ng mga elektron at butas ay pareho, kaya ang isang butas ay maaaring makunan ng isang elektron na malapit. Bilang isang resulta, ang isang atom mula sa isang positibong ion muli ay nagiging neutral. Ang proseso ng pagsasama ng mga electron na may mga butas ay tinatawag na rekombinasyon.
Sa parehong dalas, ang mga electron ay nahihiwalay mula sa mga atomo, samakatuwid, sa average, ang bilang ng mga elektron at butas para sa isang partikular na semiconductor ay pantay na, ay pare-pareho at umaasa sa mga panlabas na kondisyon, lalo na ang temperatura.
Kung ang isang boltahe ay inilalapat sa semiconductor crystal, pagkatapos ay mag-utos ang paggalaw ng elektron, isang kasalukuyang dumadaloy sa kristal dahil sa conductivity ng elektron at butas nito. Ang kondaktibiti na ito ay tinatawag na intrinsic, nabanggit na ito na medyo mataas.
Ngunit ang mga semiconductor sa kanilang purong anyo, pagkakaroon ng conductivity ng elektronik at hole, ay hindi angkop para sa paggawa ng mga diode, transistor, at iba pang mga detalye, dahil ang batayan ng mga aparatong ito ay ang p-n (basahin ang "pe-en") na kantong.
Upang makakuha ng tulad ng isang paglipat, kinakailangan ang dalawang uri ng semiconductors, dalawang uri ng kondaktibiti (p - positibo - positibo, butas) at (n - negatibo - negatibo, electronic). Ang mga uri ng semiconductors ay nakuha sa pamamagitan ng doping, pagdaragdag ng mga impurities sa purong germanium o silicon crystals.
Kahit na ang dami ng mga impurities ay napakaliit, ang kanilang pagkakaroon sa isang malaking lawak ay nagbabago sa mga katangian ng semiconductor, nagbibigay-daan sa iyo upang makakuha ng mga semiconductors ng iba't ibang kondaktibiti. Tatalakayin ito sa susunod na bahagi ng artikulo.
Boris Aladyshkin, electro-tl.tomathouse.com
Tingnan din sa electro-tl.tomathouse.com
: